Neue Fälschungsrichtlinien für Arzneimittel seit 2019 – Medikamentenfälschung verhindern
Sämtliche Arzneimittel unterliegen und benötigen höchste Sicherheit, werden aber durch Fälscher immer wieder in Gefahr gebracht. Hinter gefälschten Medikamenten können sich Arzneien mit falsch deklarierten, verdünnten oder gar fehlenden Inhaltsstoffen verbergen. Durch eine täuschend echte Verpackung oder einer Neuverpackung in Originalschachteln werden Händler und Patienten über den tatsächlichen Inhalt in die Irre geleitet. Fälschungen werden in der Regel deutlich billiger hergestellt und verkauft, als die echten Original-Präparate. Weltweit, so eine Schätzung der amerikanischen FDA (Food and Drug Administration), sollen über 10 % aller im Umlauf befindlichen Medikamente gefälscht sein. Die möglichen Folgen, die daraus resultieren: Patienten sind im Glauben die richtigen Arznei einzunehmen und nehmen unwissentlich unwirksame oder gar schädliche Stoffe bzw. Wirkstoffe ein, mit möglicherweise drastischen Folgen für ihre Gesundheit. Die von der Weltgesundheitsorganisation geforderten Fälschungsrichtlinien für Arzneimittel, die viele Staaten derzeit einführen, sind also längst überfällig – und eine rasche Compliance liegt im Interesse aller seriösen Pharmaproduzenten. Den Gefahren gefälschter Medikamente für Verbraucher und Unternehmen treten die Gesetzgeber seit einigen Jahren entschlossen durch den Erlass nationaler und supranationaler Fälschungsrichtlinien entgegen. Durch eine rasche Umsetzung der Fälschungsrichtlinien können Pharmahersteller und Verpackungsdienstleister sicherstellen, dass ihre Produkte nahtlos weiter vertrieben und gefälschte Billigprodukte (illegale Arzneimittel) zuverlässig vom Markt entfernt werden.
Ab 2019: Medikamente nur noch mit 2D Barcodes
Ab dem 9. Februar 2019 dürfen Pharmaunternehmen verschreibungspflichtige Arzneimittel nur noch mit zwei neuen Sicherheitsmerkmalen auf ihrer Verpackung in den Verkehr bringen. Jede Packung braucht dann eine individuelle Seriennummer und ein Siegel, an dem erkennbar ist, ob die Verpackung unversehrt ist. Dazu gehört als individuelles Erkennungsmerkmal ein Barcode, der sogenannte Data-Matrix-Code, den Apotheker bei der Abgabe der Medikamente scannen müssen. Damit stellen sie sicher, dass die jeweilige Packung weder gefälscht noch gestohlen ist. So kann die Echtheit einer Tablettenpackung kontrolliert werden. Ziel dieser europäischen Vorgaben aus dem Jahr 2011 ist es, Patienten vor gefälschten Arzneimitteln zu schützen. Zudem soll sich mit einem neuen, zentralen Verifizierungssystem jederzeit nachverfolgen lassen, welchen Weg jedes einzelne Medikament genommen hat, bevor es in der Apotheke landet. Dazu werden alle Medikamentendaten ab Herstellungsort in eine Datenbank übertragen, mit der am Ende alle Apotheken, Hersteller und Lieferanten verbunden und vernetzt sind. Händigen Apotheker dem Patienten ein Medikament aus, müssen sie laut der neuen EU-Verordnung anhand des aufgedruckten Datamatrix-Codes auch noch einmal zur Sicherheit prüfen, ob es sich bei dem Medikament um ein echtes handelt. Dafür müssen bis spätestens 2019 alle deutschen Apotheken über einen 2D Barcode Scanner verfügen.
Versiegelung bietet zusätzlich Schutz
In dem Code sind bei Präparaten für den deutschen Markt eine Seriennummer und ein Produktcode enthalten (mit integrierter Pharmazentralnummer), sowie die Chargennummer und das Verfallsdatum. Die Informationen müssen zusätzlich auch in Klarschrift aufgedruckt sein. Darüber hinaus muss jede Packung versiegelt werden, um zu gewährleisten, dass keine unberechtigte Entnahme – und möglicherweise Verfälschung – erfolgen kann. Die aktuelle EU-Verordnung sieht sehr detailliert vor, wo und wie die Sicherheitsmerkmale aufzubringen sind und wie die Barcode-Daten gespeichert werden – ein zum Teil nicht unerheblicher Aufwand für pharmazeutische Unternehmen, da viele interne Abläufe von dem neuen Serialisierungsprozess betroffen sind, unter anderem die IT-Abteilung, Produktion und Qualitätsmanagement.
Tamper-Evident Verschluss für 2019: Besonderheit der EU-Fälschungsrichtlinie
Der sogenannte Tamper-Evident Verschluss wird bei verschreibungspflichtigen Medikamenten in Ländern verlangt, die ab dem 9. Februar 2019 der EU-Fälschungsrichtlinie unterliegen. Das Siegel macht eine nachträgliche Manipulation des verpackten Medikamentes unmöglich oder auch das Verbergen gefälschter Medikamente in Originalverpackungen wird somit unterbunden. Wichtig ist. dass wenn das Siegel beim Verkauf beschädigt oder bereits geöffnet wurde, nicht an den Kunden weitergegeben werden darf.
Mit wenigen Ausnahmen – dürfen nur noch verschreibungspflichtige Präparate auf den Markt gebracht werden, die auf der Packung einen 2D-Barcode aufgedruckt haben. Bereits im Handel befindliche Ware darf abverkauft werden. In dem Code sind bei Präparaten für den deutschen Markt eine Seriennummer und ein Produktcode enthalten (mit integrierter Pharmazentralnummer), sowie die Chargennummer und das Verfallsdatum. Die Informationen müssen zusätzlich auch in Klarschrift aufgedruckt sein. Darüber hinaus muss jede Packung versiegelt werden, um zu gewährleisten, dass keine unberechtigte Entnahme – und möglicherweise Verfälschung – erfolgen kann.
Ein spezieller DataMatrix-Code plus Packungsversiegelung soll künftig dafür sorgen, dass Arzneimittel nicht mehr fälschbar sind.
Apotheken müssen jetzt umrüsten um für 2019 startbereit zu sein
Das Ziel der neuen Arzneifälschungsrichtlinien ist es durch die individuelle Seriennummer mit bis zu 20 Zeichen jederzeit nachvollziehbar zu machen. Somit kann jederzeit festgestellt werden, was mit einem Medikament geschehen ist, bis es schließlich in der Apotheke ankommt. Denn deren Aufgabe wird es ab 2019 sein, bei der Abgabe eines verschreibungspflichtigen Produktes an einen Patienten nochmals die Echtheit und Unversehrtheit zu prüfen – und das verpflichtend bei jeder Medikamentenverpackung! Aufgrunddessen müssen Apothekens bis 2019 alle mit einem 2D-Scanner an der Kasse ausgestattet sein. Die Software wiederum muss bis dahin fähig sein, am Verkaufstisch die erfassten Daten aus dem 2D Code in kürzester Zeit via Internet mit denen im Herstellerdatenpool abzugleichen, damit die Packung als echt freigegeben und dem Kunden ausgehändigt werden kann. Für die Apotheken wurde speziell hierfür ein getrenntes eigenes System errichtet, über das anonymisiert Anfrage und Antwort zur Herstellerdatenbank laufen. Die Seriennummer wird dann ausgetragen. Eine weitere Verwendung würde Fälschungsalarm auslösen.
Andere Länder, andere Kennzeichnung von Arzneimittel
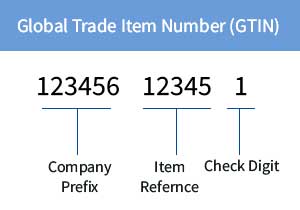
Alle Fälschungsrichtlinien benötigen eine individuelle Produkt-Identifikationsnummer auf den jeweiligen Medikamenten. Hinzu kommen beim Großteil der Richtlinien das Verfallsdatum für das Medikament, sowie eine Chargennummer und gegebenenfalls eine Seriennummer. In welchem Format diese Kennzeichnungen jedoch erfolgt, kann stark variieren. Immer enthalten sein muss aber menschenlesbare Klarschrift, sowie ein maschinenlesbarer Barcode. Ähnliches trifft auf die Art der Produkt-Identifikationsnummer zu – oftmals wird das GTIN-Format der GS1 gefordert oder auch eine ID-Nummer im NTIN oder länderspezifischen Formaten vorausgesetzt (wie z. B. PPN in Deutschland, CIP in Frankreich, KDC in Korea, CNK in Belgien, AIC in Italien usw.). In der Produkt-Identifikationsnummer sind üblicherweise folgende Informationen enthalten: Ein Länder-Präfix, die Unternehmensnummer, die Artikelnummer und eine Prüfziffer.
Die National Trade Item Number (NTIN)
Die National Trade Item Number (NTIN) ist eine global eindeutige 13-stellige Nummer im Gesundheitswesen. In Österreich ist die PZN ein Teil der NTIN (auch als PZN-EAN-Code bezeichnet). Der Aufbau der NTIN (National Trade Item Number) mit der österreichischen Pharmazentralnummer (PZN) ist in folgender Grafik ersichtlich:
Global Trade Item Number (GTIN)